Պեպտիդները միացությունների դաս են, որոնք առաջանում են պեպտիդային կապերի միջոցով բազմաթիվ ամինաթթուների միացման արդյունքում։Նրանք ամենուր տարածված են կենդանի օրգանիզմներում։Մինչ այժմ կենդանի օրգանիզմներում հայտնաբերվել են տասնյակ հազարավոր պեպտիդներ։Պեպտիդները կարևոր դեր են խաղում տարբեր համակարգերի, օրգանների, հյուսվածքների և բջիջների ֆունկցիոնալ գործունեության կարգավորման և կենսագործունեության մեջ և հաճախ օգտագործվում են ֆունկցիոնալ վերլուծության, հակամարմինների հետազոտության, դեղերի մշակման և այլ ոլորտներում:Կենսատեխնոլոգիայի և պեպտիդների սինթեզի տեխնոլոգիայի զարգացման հետ մեկտեղ ավելի ու ավելի շատ պեպտիդային դեղամիջոցներ են մշակվել և կիրառվում կլինիկայում:
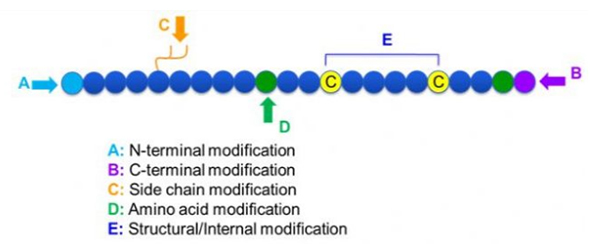
Գոյություն ունեն պեպտիդների փոփոխությունների լայն տեսականի, որոնք պարզապես կարելի է բաժանել հետմոդիֆիկացիայի և գործընթացի փոփոխության (օգտագործելով ստացված ամինաթթուների ձևափոխումը), և N-տերմինալի ձևափոխման, C-տերմինալի փոփոխության, կողային շղթայի փոփոխության, ամինաթթվի ձևափոխման, կմախքի փոփոխության, և այլն, կախված փոփոխության վայրից (Նկար 1):Որպես հիմնական շղթայի կառուցվածքը կամ պեպտիդային շղթաների կողային շղթայի խմբերը փոխելու կարևոր միջոց, պեպտիդային ձևափոխումը կարող է արդյունավետորեն փոխել պեպտիդային միացությունների ֆիզիկական և քիմիական հատկությունները, բարձրացնել ջրի լուծելիությունը, երկարացնել գործողության ժամանակը in vivo, փոխել դրանց կենսաբանական բաշխումը, վերացնել իմունոգենությունը: , նվազեցնել թունավոր կողմնակի ազդեցությունները և այլն: Այս հոդվածում ներկայացվում են պեպտիդների փոփոխման մի քանի հիմնական ռազմավարություններ և դրանց բնութագրերը:
1. Հեծանիվացում
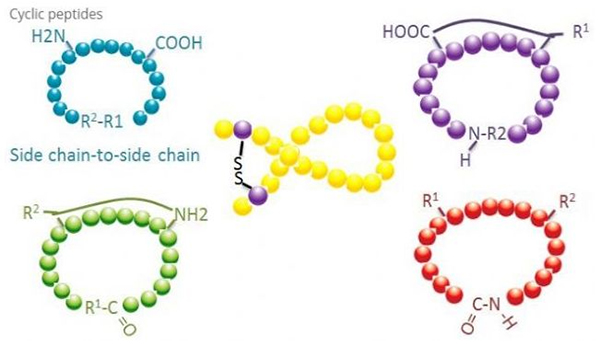
Ցիկլային պեպտիդները բազմաթիվ կիրառություններ ունեն կենսաբժշկության մեջ, և կենսաբանական ակտիվությամբ շատ բնական պեպտիդներ ցիկլային պեպտիդներ են:Քանի որ ցիկլային պեպտիդները հակված են ավելի կոշտ լինել, քան գծային պեպտիդները, նրանք չափազանց դիմացկուն են մարսողական համակարգի նկատմամբ, կարող են գոյատևել մարսողական տրակտում և ավելի ուժեղ մերձություն ցուցաբերել թիրախային ընկալիչների նկատմամբ:Ցիկլիզացիան ցիկլային պեպտիդների սինթեզման ամենաուղղակի միջոցն է, հատկապես մեծ կառուցվածքային կմախք ունեցող պեպտիդների համար։Ըստ ցիկլացման ռեժիմի՝ այն կարելի է բաժանել կողային շղթայի կողային շղթայի տիպի, տերմինալ-կողային շղթայի տիպի, տերմինալ-տերմինալի տիպի (վերջից ծայր տիպ):
(1) sidechain-to-sidechain
Կողային շղթայից դեպի կողային շղթա ցիկլացման ամենատարածված տեսակը ցիստեինի մնացորդների միջև դիսուլֆիդային կամրջումն է:Այս ցիկլացումը ներմուծվում է ցիստեինի մի զույգ մնացորդների կողմից, որոնք ապապաշտպանվում են, իսկ հետո օքսիդացվում են դիսուլֆիդային կապեր ձևավորելու համար:Պոլիկիկլիկ սինթեզը կարող է իրականացվել սուլֆիհիդրիլային պաշտպանության խմբերի ընտրովի հեռացման միջոցով:Ցիկլիզացիան կարող է իրականացվել կա՛մ հետդիսոցացիոն լուծիչի մեջ, կա՛մ նախաքննական խեժի վրա:Խեժերի վրա ցիկլացումը կարող է ավելի քիչ արդյունավետ լինել, քան լուծիչի ցիկլացումը, քանի որ խեժերի վրա պեպտիդները հեշտությամբ չեն ձևավորում ցիկլացված կոնֆորմացիաներ:Կողմնակի շղթայի մեկ այլ տեսակ՝ կողային շղթայի ցիկլացումը, ասպարթաթթվի կամ գլուտամինաթթվի մնացորդի և բազային ամինաթթվի միջև ամիդային կառուցվածքի ձևավորումն է, որը պահանջում է, որ կողմնակի շղթայի պաշտպանության խումբը պետք է կարողանա ընտրովիորեն հեռացնել պոլիպեպտիդից։ խեժի վրա կամ տարանջատումից հետո:Կողմնակի շղթայի երրորդ տեսակը՝ կողային շղթայի ցիկլացումը, դիֆենիլ եթերների ձևավորումն է թիրոզինի կամ պ-հիդրօքսիֆենիլգլիցինի կողմից։Բնական արտադրանքներում ցիկլացման այս տեսակը հանդիպում է միայն մանրէաբանական արտադրանքներում, և ցիկլացման արտադրանքը հաճախ ունի պոտենցիալ բժշկական արժեք:Այս միացությունների պատրաստումը պահանջում է ռեակցիայի յուրահատուկ պայմաններ, ուստի դրանք հաճախ չեն օգտագործվում սովորական պեպտիդների սինթեզում։
(2) տերմինալ-կողային շղթա
Տերմինալ-կողային շղթայի ցիկլացումը սովորաբար ներառում է C-տերմինալը լիզինի կամ օրնիտինի կողային շղթայի ամինո խմբի հետ, կամ N-տերմինալը ասպարթաթթվի կամ գլուտամինաթթվի կողային շղթայի հետ:Պոլիպեպտիդների այլ ցիկլացումն իրականացվում է եթերային կապեր ձևավորելով C տերմինալի և սերինի կամ թրեոնինի կողային շղթաների միջև:
(3) Տերմինալ կամ գլխից պոչ տեսակ
Շղթայական պոլիպեպտիդները կարող են կամ ցիկլվել լուծիչի մեջ կամ ամրագրվել խեժի վրա կողային շղթայական ցիկլացիայի միջոցով:Պեպտիդների ցածր կոնցենտրացիաները պետք է օգտագործվեն լուծիչների կենտրոնացման ժամանակ՝ պեպտիդների օլիգոմերացումից խուսափելու համար:Գլխից պոչ սինթետիկ օղակաձեւ պոլիպեպտիդի ելքը կախված է շղթայի պոլիպեպտիդի հաջորդականությունից:Հետևաբար, նախքան ցիկլային պեպտիդները մեծ մասշտաբով պատրաստելը, նախ պետք է ստեղծել հնարավոր շղթայական կապարի պեպտիդների գրադարան, որին հաջորդում է ցիկլացումը՝ լավագույն արդյունքներով հաջորդականությունը գտնելու համար:
2. N-մեթիլացում
N-մեթիլացումը սկզբնապես տեղի է ունենում բնական պեպտիդներում և ներմուծվում է պեպտիդների սինթեզի մեջ՝ կանխելու ջրածնային կապերի ձևավորումը՝ դրանով իսկ պեպտիդները դարձնելով ավելի դիմացկուն կենսաքայքայման և մաքրման նկատմամբ:Պեպտիդների սինթեզը՝ օգտագործելով N-մեթիլացված ամինաթթուների ածանցյալները, ամենակարևոր մեթոդն է։Բացի այդ, կարող է օգտագործվել նաև N-(2-նիտրոբենզոլ սուլֆոնիլքլորիդ) պոլիպեպտիդ-խեժի միջանկյալ նյութերի Mitsunobu ռեակցիան մեթանոլով:Այս մեթոդը օգտագործվել է N-մեթիլացված ամինաթթուներ պարունակող ցիկլային պեպտիդային գրադարաններ պատրաստելու համար:
3. Ֆոսֆորիլացում
Ֆոսֆորիլացումը բնության մեջ ամենատարածված հետթարգմանական փոփոխություններից մեկն է:Մարդու բջիջներում սպիտակուցների ավելի քան 30%-ը ֆոսֆորիլացված է։Ֆոսֆորիլացումը, հատկապես շրջելի ֆոսֆորիլացումը, կարևոր դեր է խաղում բազմաթիվ բջջային պրոցեսների վերահսկման գործում, ինչպիսիք են ազդանշանի փոխակերպումը, գեների էքսպրեսիան, բջջային ցիկլի և ցիտոկմախքի կարգավորումը և ապոպտոզը:
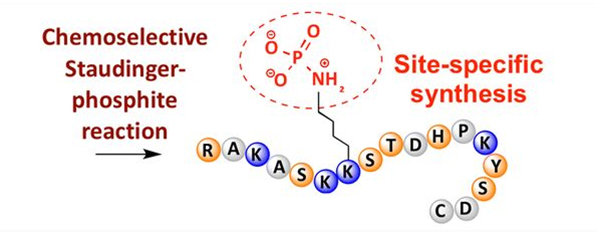
Ֆոսֆորիլացումը կարող է դիտվել ամինաթթուների մի շարք մնացորդներում, սակայն ֆոսֆորիլացման ամենատարածված թիրախներն են սերինը, թրեոնինը և թիրոզինի մնացորդները:Ֆոսֆոտիրոզին, ֆոսֆոտրեոնին և ֆոսֆոսերինի ածանցյալները կարող են կամ ներմուծվել պեպտիդների մեջ սինթեզի ընթացքում կամ ձևավորվել պեպտիդների սինթեզից հետո:Ընտրովի ֆոսֆորիլացումը կարող է իրականացվել՝ օգտագործելով սերինի, թրեոնինի և թիրոզինի մնացորդները, որոնք ընտրողաբար հեռացնում են պաշտպանիչ խմբերը:Որոշ ֆոսֆորիլացման ռեակտիվներ կարող են նաև ֆոսֆորաթթվի խմբեր ներմուծել պոլիպեպտիդ՝ հետմոդիֆիկացիայի միջոցով:Վերջին տարիներին լիզինի տեղային հատուկ ֆոսֆորիլացումը ձեռք է բերվել քիմիապես ընտրովի Շտաուդինգեր-ֆոսֆիտ ռեակցիայի միջոցով (Նկար 3):
4. Myristoylation եւ palmitoylation
N-տերմինալի ացիլացումը ճարպաթթուներով թույլ է տալիս պեպտիդներին կամ սպիտակուցներին միանալ բջջային թաղանթներին:N-տերմինալի վրա միրիդամոիլացված հաջորդականությունը հնարավորություն է տալիս Src ընտանիքի պրոտեին կինազներին և հակադարձ տրանսկրիպտազային Gaq սպիտակուցներին թիրախավորել բջջային թաղանթներին միանալու համար:Միրիստիկ թթուն կապվել է խեժ-պոլիպեպտիդի N-տերմինալի հետ՝ օգտագործելով ստանդարտ զուգավորման ռեակցիաներ, և ստացված լիպոպեպտիդը կարող է տարանջատվել ստանդարտ պայմաններում և մաքրվել RP-HPLC-ով:
5. Գլիկոզիլացում
Գլիկոպեպտիդները, ինչպիսիք են վանկոմիցինը և տեյկոլանինը, կարևոր հակաբիոտիկներ են դեղակայուն բակտերիալ վարակների բուժման համար, իսկ այլ գլիկոպեպտիդներ հաճախ օգտագործվում են իմունային համակարգը խթանելու համար:Բացի այդ, քանի որ շատ մանրէաբանական անտիգեններ գլիկոզիլացված են, մեծ նշանակություն ունի գլիկոպեպտիդների ուսումնասիրությունը՝ վարակի թերապևտիկ ազդեցությունը բարելավելու համար:Մյուս կողմից, պարզվել է, որ ուռուցքային բջիջների բջջային թաղանթի վրա գտնվող սպիտակուցները ցուցադրում են աննորմալ գլիկոզիլացում, ինչը գլիկոպեպտիդներին դարձնում է կարևոր դեր քաղցկեղի և ուռուցքի իմունային պաշտպանության հետազոտություններում:Գլիկոպեպտիդները պատրաստվում են Fmoc/t-Bu մեթոդով։Գլիկոզիլացված մնացորդները, ինչպիսիք են թրեոնինը և սերինը, հաճախ ներմուծվում են պոլիպեպտիդների մեջ պենտաֆտորֆենոլ էսթերով ակտիվացված fMOC-ներով՝ գլիկոզիլացված ամինաթթուները պաշտպանելու համար:
6. Իզոպրեն
Իզոպենտադիենիլացումը տեղի է ունենում C-տերմինալի մոտ գտնվող կողային շղթայում ցիստեինի մնացորդների վրա:Սպիտակուցային իզոպրենը կարող է բարելավել բջջային մեմբրանի մերձեցումը և ձևավորել սպիտակուց-սպիտակուց փոխազդեցություն:Իզոպենտադիենացված սպիտակուցները ներառում են թիրոզինֆոսֆատազ, փոքր GTase, կոկապերոնի մոլեկուլներ, միջուկային շերտ և ցենտրոմերային կապող սպիտակուցներ։Իզոպրենային պոլիպեպտիդները կարող են պատրաստվել խեժերի վրա իզոպրեն օգտագործելով կամ ցիստեինի ածանցյալներ ներմուծելով:
7. Պոլիէթիլեն գլիկոլի (PEG) փոփոխություն
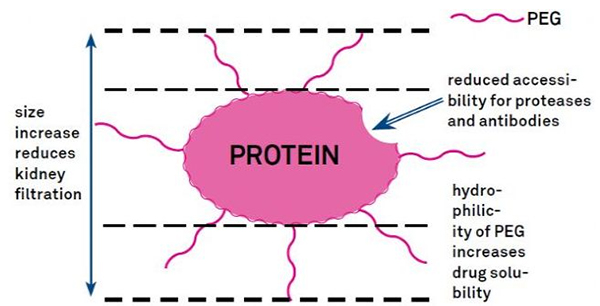
PEG-ի ձևափոխումը կարող է օգտագործվել սպիտակուցի հիդրոլիտիկ կայունությունը, կենսաբաշխումը և պեպտիդների լուծելիությունը բարելավելու համար:PEG շղթաների ներմուծումը պեպտիդներին կարող է բարելավել դրանց դեղաբանական հատկությունները և նաև արգելակել պրոտեոլիտիկ ֆերմենտների կողմից պեպտիդների հիդրոլիզը:PEG պեպտիդները ավելի հեշտ են անցնում գնդիկավոր մազանոթների խաչմերուկով, քան սովորական պեպտիդները, ինչը զգալիորեն նվազեցնում է երիկամների մաքրումը:PEG պեպտիդների երկարացված ակտիվ կիսամյակի շնորհիվ in vivo-ում, բուժման նորմալ մակարդակը կարող է պահպանվել ավելի ցածր չափաբաժիններով և ավելի քիչ հաճախակի պեպտիդային դեղամիջոցներով:Այնուամենայնիվ, PEG-ի մոդիֆիկացիան ունի նաև բացասական ազդեցություն:PEG-ի մեծ քանակությունը կանխում է ֆերմենտի քայքայումը պեպտիդը և նաև նվազեցնում է պեպտիդի կապը թիրախային ընկալիչի հետ:Սակայն PEG պեպտիդների ցածր մերձեցումը սովորաբար փոխհատուցվում է նրանց ավելի երկար ֆարմակոկինետիկ կիսամյակի շնորհիվ, և մարմնում ավելի երկար լինելով՝ PEG պեպտիդները թիրախ հյուսվածքներում ներծծվելու ավելի մեծ հավանականություն ունեն:Հետևաբար, PEG պոլիմերային բնութագրերը պետք է օպտիմալացվեն օպտիմալ արդյունքների համար:Մյուս կողմից, PEG պեպտիդները կուտակվում են լյարդում՝ երիկամային մաքրման նվազեցման պատճառով, ինչը հանգեցնում է մակրոմոլեկուլային համախտանիշի:Հետևաբար, PEG-ի փոփոխությունները պետք է մշակվեն ավելի ուշադիր, երբ պեպտիդներն օգտագործվում են դեղերի փորձարկման համար:
PEG մոդիֆիկատորների ընդհանուր մոդիֆիկացիոն խմբերը կարելի է մոտավորապես ամփոփել հետևյալ կերպ. Ամինո (-ամին) -NH2, ամինոմեթիլ-Ch2-NH2, հիդրօքսի-OH, կարբոքսի-Cooh, սուլֆհիդրիլ (-Թիոլ) -SH, մալեյիմիդ -MAL, սուկցինիմիդ կարբոնատ - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (օրինակ՝ propional-ald, butyrALD), ակրիլային հիմք (-acrylate-acrl), azido-inylazide, Biotin, Fluorescein, glutaryl-GA, Acrylate Hydrazide, alkyne-alkyne, p-toluenesulfonate -OTs, succinimide succinate -SS և այլն: PEG ածանցյալները կարբոքսիլաթթուներով կարող են զուգակցվել n-տերմինալ ամինների կամ լիզինի կողային շղթաների հետ:Ամինաակտիվացված PEG-ը կարող է զուգակցվել ասպարտաթթվի կամ գլուտամինաթթվի կողմնակի շղթաների հետ:Սխալ ակտիվացված PEG-ը կարող է զուգակցվել լիովին ապապաշտպանված ցիստեինի կողմնակի շղթաների մերկապտանին [11]:PEG մոդիֆիկատորները սովորաբար դասակարգվում են հետևյալ կերպ (նշում. mPEG-ը մետօքսի-PEG է, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) ուղիղ շղթայի PEG փոփոխիչ
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) երկֆունկցիոնալ PEG փոփոխիչ
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) ճյուղավորվող PEG փոփոխիչ
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Բիոտինացում
Բիոտինը կարող է ամուր կապված լինել ավիդինի կամ streptavidin-ի հետ, և կապող ուժը նույնիսկ մոտ է կովալենտային կապին:Բիոտինով պիտակավորված պեպտիդները սովորաբար օգտագործվում են իմունային հետազոտության, հիստոցիտոքիմիայի և ֆլյուորեսցենցիայի վրա հիմնված հոսքի բջջաչափության մեջ:Պիտակավորված հակաբիոտինային հակամարմինները կարող են օգտագործվել նաև բիոտինիլացված պեպտիդները կապելու համար:Բիոտինի պիտակները հաճախ կցվում են լիզինի կողային շղթային կամ N տերմինալին:6-aminocaproic թթուն հաճախ օգտագործվում է որպես կապ պեպտիդների և բիոտինի միջև:Կապը ճկուն է սուբստրատի հետ կապելու մեջ և ավելի լավ է կապվում ստերիկ խոչընդոտների առկայության դեպքում:
9. Լյումինեսցենտային պիտակավորում
Լյումինեսցենտային պիտակավորումը կարող է օգտագործվել կենդանի բջիջներում պոլիպեպտիդների հետքի և ֆերմենտների և գործողության մեխանիզմների ուսումնասիրության համար:Տրիպտոֆանը (Trp) լյումինեսցենտ է, ուստի այն կարող է օգտագործվել ներքին պիտակավորման համար:Տրիպտոֆանի արտանետումների սպեկտրը կախված է ծայրամասային միջավայրից և նվազում է լուծիչի բևեռականության նվազմամբ, հատկություն, որն օգտակար է պեպտիդների կառուցվածքը և ընկալիչների կապը հայտնաբերելու համար:Տրիպտոֆանի ֆլուորեսցենցիան կարող է մարվել պրոտոնացված ասպարտիկ թթվի և գլուտամինաթթվի միջոցով, ինչը կարող է սահմանափակել դրա օգտագործումը:Դանսիլ քլորիդ խումբը (Dansyl) շատ լյումինեսցենտ է, երբ կապված է ամինային խմբի հետ և հաճախ օգտագործվում է որպես ամինաթթուների կամ սպիտակուցների լյումինեսցենտային պիտակ:
Ֆլյուորեսցենտային ռեզոնանսային էներգիայի փոխակերպումը (FRET) օգտակար է ֆերմենտային ուսումնասիրությունների համար:Երբ FRET-ը կիրառվում է, ենթաշերտի պոլիպեպտիդը սովորաբար պարունակում է ֆլյուորեսցենտային պիտակավորման խումբ և լյումինեսցենտային հանգցնող խումբ:Նշված լյումինեսցենտային խմբերը մարվում են հանգցնողի կողմից ոչ ֆոտոտոնային էներգիայի փոխանցման միջոցով:Երբ պեպտիդը տարանջատվում է տվյալ ֆերմենտից, պիտակավորման խումբն արտանետում է ֆլյուորեսցենտ:
10. Վանդակի պոլիպեպտիդներ
Վանդակի պեպտիդներն ունեն օպտիկականորեն շարժական պաշտպանիչ խմբեր, որոնք պաշտպանում են պեպտիդը ընկալիչի հետ կապվելուց:Ուլտրամանուշակագույն ճառագայթման ենթարկվելիս պեպտիդն ակտիվանում է՝ վերականգնելով իր կապը ընկալիչի հետ:Քանի որ այս օպտիկական ակտիվացումը կարող է վերահսկվել ըստ ժամանակի, ամպլիտուդի կամ գտնվելու վայրի, վանդակի պեպտիդները կարող են օգտագործվել բջիջներում տեղի ունեցող ռեակցիաները ուսումնասիրելու համար:Վանդակի պոլիպեպտիդների համար առավել հաճախ օգտագործվող պաշտպանիչ խմբերը 2-նիտրոբենզիլային խմբերն են և դրանց ածանցյալները, որոնք կարող են ներդրվել պեպտիդների սինթեզում պաշտպանիչ ամինաթթուների ածանցյալների միջոցով:Ամինաթթուների ածանցյալներն են՝ լիզինը, ցիստեինը, սերինը և թիրոզինը։Ասպարտատի և գլյուտամատի ածանցյալները, սակայն, սովորաբար չեն օգտագործվում պեպտիդների սինթեզի և տարանջատման ընթացքում ցիկլացման նկատմամբ իրենց զգայունության պատճառով:
11. Պոլյանտիգեն պեպտիդ (MAP)
Կարճ պեպտիդները սովորաբար անձեռնմխելի չեն և պետք է զուգակցվեն կրող սպիտակուցների հետ՝ հակամարմիններ արտադրելու համար:Պոլյանտիգենային պեպտիդը (MAP) բաղկացած է մի քանի նույնական պեպտիդներից, որոնք կապված են լիզինի միջուկների հետ, որոնք կարող են հատուկ արտահայտել բարձր հզորության իմունոգեններ և կարող են օգտագործվել պեպտիդ-կրիչ սպիտակուցի երկտողեր պատրաստելու համար:MAP պոլիպեպտիդները կարող են սինթեզվել MAP խեժի վրա պինդ փուլային սինթեզի միջոցով:Այնուամենայնիվ, թերի զուգավորումը հանգեցնում է որոշ ճյուղերի պեպտիդային շղթաների բացակայման կամ կտրվածության, և, հետևաբար, չի ցուցադրում բնօրինակ MAP պոլիպեպտիդի հատկությունները:Որպես այլընտրանք, պեպտիդները կարող են պատրաստվել և զտվել առանձին, այնուհետև միացնել MAP-ին:Պեպտիդային հաջորդականությունը, որը կցված է պեպտիդային միջուկին, լավ սահմանված է և հեշտությամբ բնութագրվում է զանգվածային սպեկտրաչափությամբ:
Եզրակացություն
Պեպտիդների ձևափոխումը պեպտիդների նախագծման կարևոր միջոց է:Քիմիապես ձևափոխված պեպտիդները կարող են ոչ միայն պահպանել բարձր կենսաբանական ակտիվություն, այլև արդյունավետորեն խուսափել իմունոգենության և թունավորության թերություններից:Միևնույն ժամանակ, քիմիական մոդիֆիկացիան կարող է պեպտիդներին օժտել մի քանի նոր հիանալի հատկություններով:Վերջին տարիներին արագորեն մշակվել է պոլիպեպտիդների հետմոդիֆիկացիայի համար CH-ի ակտիվացման մեթոդը, և ձեռք են բերվել շատ կարևոր արդյունքներ:
Հրապարակման ժամանակը՝ Մար-20-2023
